 شرکت در آزمون آنلاین
شیمی 3
-
فصل 4: شیمی، راهی به سوی آینده ای روشن تر
| آزمون شماره 487
شرکت در آزمون آنلاین
شیمی 3
-
فصل 4: شیمی، راهی به سوی آینده ای روشن تر
| آزمون شماره 487
مطابق اصل لوشاتلیه می توان گفت: .........................
تعادل گازی $CO\left( g \right)+۳{{H}_{۲}}\left( g \right)\rightleftharpoons C{{H}_{۴}}\left( g \right)+{{H}_{۲}}O\left( g \right)$ در دمای معین در یک ظرف با وارد کردن مقداری گاز $CO$ و ${{H}_{۲}}$ برقرار شده است. مقادیر $CO$، ${{H}_{۲}}$ و $C{{H}_{۴}}$ در حال تعادل به ترتیب یرایر $۰/۸$، $۰/۴$ و $۰/۶$ مولار است، اگر ثابت تعادل در این سامانه برابر $۱۱۲/۵\ mo{{l}^{-۲}}.{{L}^{۲}}$ باشد، حجم ظرف مورد آزمایش چند لیتر است؟
چه تعداد از موارد زیر درست میباشند؟
هر چه انرژی فعالسازی واکنش بیشتر باشد، سرعت واکنش بیشتر است.
هر چه انرژی فعالسازی واکنش بیشتر باشد، آنتالپی واکنش کمتر است.
همه واکنشهای شیمیایی چه گرماگیر و چه گرماده به انرژی فعالسازی نیاز دارند.
استفاده از کاتالیزگر از نظر توسعه پایدار مطلوب به نظر میرسد.
واکنشهایی که انرژی فعالسازی زیادی دارند را نمیتوان در دما و فشار پایین انجام داد.
تفاوت محتوای انرژی واکنش دهندهها و فراوردهها در واکنشهای گرماده بیشتر از واکنشهای گرماگیر است.
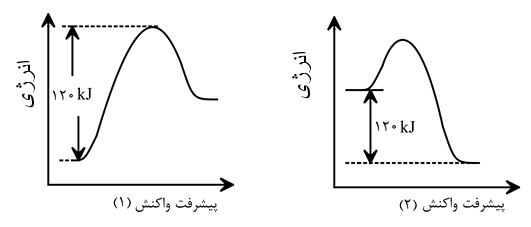 با توجه به نمودارهای زیر کدام گزینه درست است؟
با توجه به نمودارهای زیر کدام گزینه درست است؟
مخلوطی شامل ۳ مول آمونیاک، ۲ مول ${{N}_{۲}}$ و ۶ مول ${{H}_{۲}}$ در دمای ${{۱۰۰}^{۰}}C$ و در ظرفی به حجم ۱۰ لیتر در تعادل: ${{N}_{۲}}(g)+۳{{H}_{۲}}(g)\rightleftharpoons ۲N{{H}_{۳}}(g)$ قرار دارند. اگر دما به ${{۵۰۰}^{۰}}C$ افزایش یابد چه تعداد از عبارتهای زیر میتوانند درست باشند؟ $(H=۱,N=۱۴:g.mo{{l}^{-۱}})$
آ) درصد مولی آمونیاک در مخلوط تعادلی با دمای ${{۵۰۰}^{۰}}C$ به حدود ۲۸ درصد خواهد رسید.
ب) مقدار ثابت تعادل در دمای ${{۵۰۰}^{۰}}C$ کمتر از ۰۲/۰ خواهد بود.
پ) شمار مولکولهای سامانه تعادلی در ${{۵۰۰}^{۰}}C$ نسبت به سامانه تعادلی اولیه کمتر از یک خواهد بود.
ت) مجموع جرم واکنش دهندهها در مخلوط تعادلی ${{۵۰۰}^{۰}}C$ کمتر از ۶۸ گرم خواهد بود.


