 شرکت در آزمون آنلاین
شیمی 3
-
فصل 4: شیمی، راهی به سوی آینده ای روشن تر
| آزمون شماره 887
شرکت در آزمون آنلاین
شیمی 3
-
فصل 4: شیمی، راهی به سوی آینده ای روشن تر
| آزمون شماره 887
اگر در تعادل گازی $N_۲(g)+۳H_۲(g)\leftrightharpoons\ ۲NH_۳\ (g)$ که در یک ظرف سربستهی ۷ لیتری انجام میشود، در ابتدا ۱۰/۸ گرم هیدروژن به همراه مقدار کافی نیتروژن وارد ظرف شده و ۳/۰۶ گرم آمونیاک تا لحظهی تعادل حاصل شود، بازده درصدی این واکنش کدام است؟
اگر معادله شیمیایی یک واکنش تعادلی از جمع معادلههای شیمیایی دو یا چند تعادل دیگر به دست آید، ثابت تعادل واکنشش تعادلی .................. $\Delta H$ آن برابر .......................
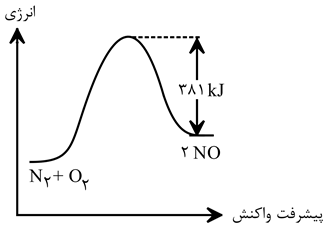 اگر ضمن تولید $۴$ گرم نیتروژن مونوکسید مطابق واکنش:${{N}_{۲}}(g)+{{O}_{۲}}(g)\to۲ NO(g)$ آنتالپی فراورده به اندازه $۱۲$ کیلوژول افزایش یابد، انرژی فعالسازی واکنش در نمودار مقابل، چند کیلوژول خواهد بود؟ $(N=۱۴,O=۱۶:g.mo{{l}^{-۱}})$
اگر ضمن تولید $۴$ گرم نیتروژن مونوکسید مطابق واکنش:${{N}_{۲}}(g)+{{O}_{۲}}(g)\to۲ NO(g)$ آنتالپی فراورده به اندازه $۱۲$ کیلوژول افزایش یابد، انرژی فعالسازی واکنش در نمودار مقابل، چند کیلوژول خواهد بود؟ $(N=۱۴,O=۱۶:g.mo{{l}^{-۱}})$
در کدامیک از تعادلهای زیر برای تولید فراورده بیشتر باید فشار کم و دما افزایش یابد؟
درباره سرعت واکنش گاز هیدروژن با گاز اکسیژن، سرعت واکنش در کدام ردیف (ها) درست اشاره شده است؟
|
ردیف |
شرایط آزمایش |
دما $\left( ^{\circ }C \right)$ |
سرعت واکنش |
آنتالپی واکنش |
|
۱ |
بدون حضور کاتالیزگر |
۲۵ |
ناچیز |
۵۷۲- |
|
۲ |
ایجاد جرقه در مخلوط |
۲۵ |
انفجاری |
۵۷۲- |
|
۳ |
در حضور پودر روی |
۲۵ |
انفجاری |
۵۷۲- |
|
۴ |
در حضور توری پلاتینی |
۲۵ |
سریع |
۵۷۲- |


