 شرکت در آزمون آنلاین
شیمی 1
-
غلظت مولی (مولار) و مسائل آن
| آزمون شماره 864
شرکت در آزمون آنلاین
شیمی 1
-
غلظت مولی (مولار) و مسائل آن
| آزمون شماره 864
دستگاه اندازهگیری قند خون، قندخون یک فرد را $95\frac{{mg}}{{dL}}$ نشان میدهد. غلظت مولی گلوکز در خون این فرد به تقریب چند $\frac{{mol}}{L}$ است؟ $({C_6}{H_{12}}{O_6} = 180\frac{g}{{mol}})$
درصدجرمی$X$ درمحلولی حاوی آن برابر $۶۳ $ است. اگرچگالی این محلول برابر $۱/۲\frac{g}{L}$ باشد، مولاریته آن کدام است؟
$\left ( X=۷۰g.mol^{-۱} \right )$
با $۸۰$ گرم محلول $۴۰$ درصدجرمی سدیم هیدروکسید، چندمیلی لیتر محلول $۳/۲\frac{mol}{L}$ سدیم هیدروکسید را میتوان تهیه کرد؟
$\left ( O=۱۶,H=۱,Na=۲۳:\frac{g}{mol} \right )$
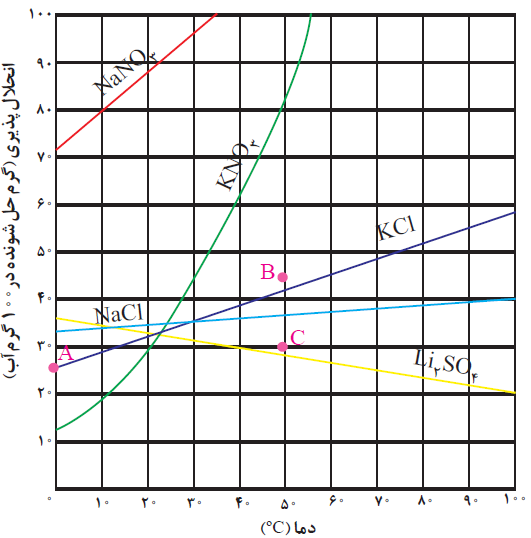
با توجه به نمودار روبرو محلول سیرشدهای از پتاسیم نیترات در $۷۰۰$ گرم آب در دمای $۵۰^{\circ }C$ تهیه شده است. در چه دمایی غلظت پتاسیم نیترات به حدود $۲\frac{mol}{L}$ میرسد و در این دما چند گرم از این نمک رسوب میکند؟ (گزینه ها را از راست به چپ بخوانید، از تغییر حجم صرف نظر کنید و چگالی محلول را $۱\, g.mL^{-۱}$ در نظر بگیرید.)
$ ۰/۳۲$ گرم مس خالص با نیتریک اسید مطابق معادله شیمیایی زیر به طور کامل واکنش میدهد:
$C{{u}_{\left( s \right)}}+HN{{O}_{۳\left( aq \right)}}\to Cu\left( N{{O}_{۳}} \right.{{)}_{۲\left( aq \right)}}+N{{O}_{۲\left( g \right)}}+{{H}_{۲}}{{O}_{\left( l \right)}}~\left( \text{معادله}~\text{موازنه}~\text{شود} \right)$
در صورتی که حجم محیط آزمایشگاه $۴۰۰$ متر مکعب و چگالی هوا در شرایط آزمایش $۱/۲$ گرم بر لیتر باشد، غلظت گاز $N{{O}_{۲}}$ در آزمایشگاه به تقریب چند $ppm$ خواهد شد؟
$\left( N=۱۴,~~O=۱۶,~~Cu=۶۴g.mo{{l}^{-۱}} \right)$


