 شرکت در آزمون آنلاین
شیمی 3
-
درجه یونش اسیدها
| آزمون شماره 4244
شرکت در آزمون آنلاین
شیمی 3
-
درجه یونش اسیدها
| آزمون شماره 4244
درصد یونش محلول 1 مولار اسید HA برابر 4% است. اگر 500 مولکول HA را به مقدار کافی آب اضافه کنیم و محلول 1 مولار HA در آب ایجاد شود، تعداد ذرههای موجود پس از حل شدن اسید در آب، کدام است؟
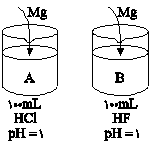
با توجه به شکل مقابل که مربوط به واکنش فلز منیزیم با محلولهای داده شدة هیدروکلریک اسید و هیدروفلوئوریکاسید است، چند مورد از مقایسههای زیر نادرست است؟
( مقدار فلز منیزیم مصرفی محلولها: $A = B$
( حجم گاز هیدروژن تولید شده: $B < A$
( سرعت واکنش منیزیم $A > B$
انحلال چه تعداد از ترکیبات زیر در آب تولید یون کرده اما، انحلال آن را نمی توان به عنوان فرایند یونش در نظر گرفت؟
$C_{۲}^{}H_{۵}^{}OH,C_{۶}^{}H_{۱۲}^{}O_{۶}^{},C_{۲}^{}H_{۴}$ ,استون, $Al_{۲}^{}O_{۳}^{},CH_{۳}^{}COOH,NaOH,NH_{۳}^{},SO_{۳}^{},CO,N_{۲}^{}O_{۵}^{}$
چگالی گاز اسیدی $HA$در دمای $۹۱^{\circ}C$ و فشار $۰/۶۶۷ atm$ برابر $۰/۶۰ g.L^{-۱}$ است. اگر ۸/۱ گرم از این گاز را در مقداری آب حل کرده و حجم محلول حاصل را به ۱۲ لیتر برسانیم، غلظت مولی یونهای هیدرونیوم موجود در محلول برابر $۱/۵\times۱۰^{-۳} mol.L^{-۱}$ میشود. درصد یونش اسید $HA$کدام است؟
درجهی یونش کدامیک از محلولهای زیر کوچکتر است؟ (ترکیبات داده شده در دمای یکسان مورد مقایسه میباشند)


