 شرکت در آزمون آنلاین
شیمی 3
-
اسیدها و بازها
| آزمون شماره 2151
شرکت در آزمون آنلاین
شیمی 3
-
اسیدها و بازها
| آزمون شماره 2151
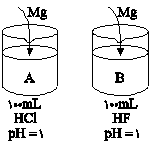
با توجه به شکل مقابل که مربوط به واکنش فلز منیزیم با محلولهای داده شدة هیدروکلریک اسید و هیدروفلوئوریکاسید است، چند مورد از مقایسههای زیر نادرست است؟
( مقدار فلز منیزیم مصرفی محلولها: $A = B$
( حجم گاز هیدروژن تولید شده: $B < A$
( سرعت واکنش منیزیم $A > B$
غلظت مولار یون هیدرونیوم در$۱۰۰$ میلیلیتر از محلول اسید ضعیف $HA$چقدر باشد تا بتوان با آن $۱۵۰$میلیلیتر محلول $۰/۱$ مولار $HA$ تهیه کرد؟ (درصد یونش $HA$ برابر $۳$ درصد است)
چند گرم $KOH$ به $۲۵۰$ میلی لیتر آب افزوده شود تا $pH$ محلول برابر $۱۳$ گردد؟ ($\text{KOH}=۵۶\text{ }\!\!~\!\!\text{ g}.\text{mo}{{\text{l}}^{-۱}}$)
چه تعداد از مطالب زیر درست هستند؟
آ) اسید درون معده میتواند فلز روی را در خود حل کند.
ب) آسپرین با فرمول مولکولی ${{C}_{8}}{{H}_{8}}{{O}_{4}}$ سبب تشدید سوزش معده و خونریزی آن میشود.
پ) در واکنش ماده اصلی شیر منیزی و اسید معده پس از موازنه، مجموع ضرایب واکنشدهندهها و فراوردهها برابر 6 است.
ت) سدیم هیدروژنکربنات (جوش شیرین) یک اسید آرنیوس است؛ به همین علت برای افزایش قدرت پاککنندگی به شویندهها اضافه میشود.
کدام مطلب زیر، درست اند؟
آ) همه بازهای آرنیوس در ساختار خود یون هیدروکسید $(O{{H}^{-}})$ دارند.
ب) تعریف آرنیوس برای اسیدها یا بازها، به محلول های آبی محدود می شود.
پ) 0/5 مول سولفوریک اسید با 0/8 مول سدیم هیدروکسید، خنثی می شود.
ت) معادله یونش $HN{{O}_{3}}$ یک طرفه، ولی معادله یونش HCN برگشت پذیر است.


