 شرکت در آزمون آنلاین
شیمی 3
-
درجه یونش اسیدها
| آزمون شماره 4190
شرکت در آزمون آنلاین
شیمی 3
-
درجه یونش اسیدها
| آزمون شماره 4190
کدامیک از عبارتهای زیر درست میباشد؟
$۲$ مول اسید ضعیف $HX$در مقدار زیادی آب حل شده و مجموع شمار ذرات یونیده شده و یونیده نشده حاصل از آن در محلول برابر $۱۵/۰۵\times{۱۰}^{۲۳}$شده است. در این صورت درصد یونش $HX$ کدام است؟
با توجه به نمودارهای زیر که غلظت نسبی گونههای موجود در محلولهای آبی یک مولار با حجم یكسان از دو اسید $HA$ و $HX$ را پیش و پس از یونش نشان میدهند، چند مورد از مطالب زیر درستاند؟
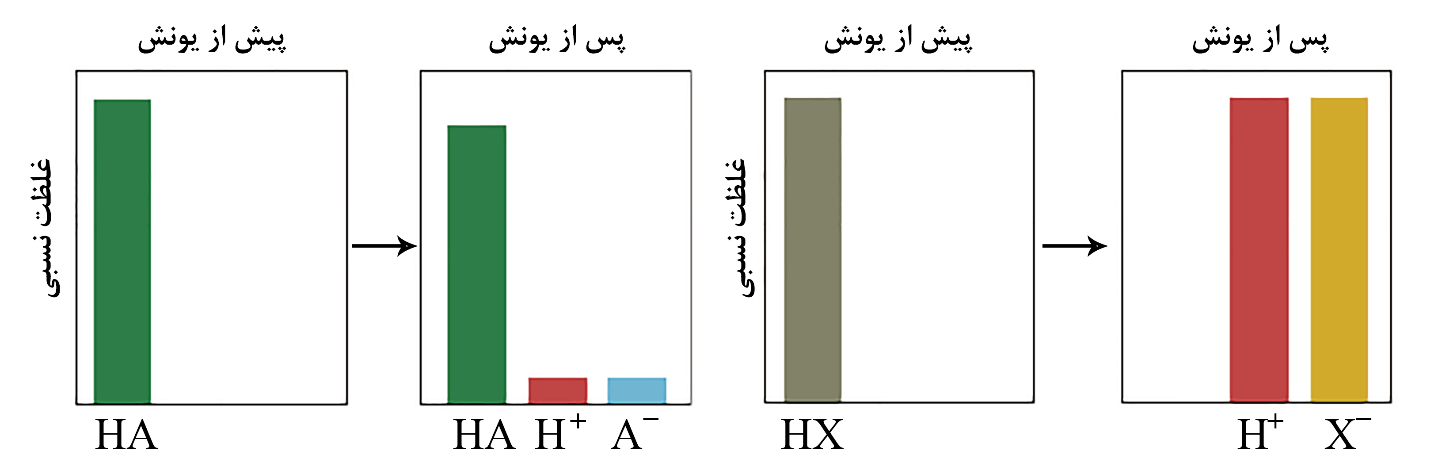

تفاوت غلظت یون هیدرونیوم با غلظت اولیۀ اسید در محلول $HA$ از محلول $HX$ بیشتر است.
در شرایط یکسان سرعت واکنش دو قطعۀ مشابه منیزیمی با دو محلول $HA$ و $HX$ بطور چشمگیری متفاوت است.
در دمای یكسان، رسانایی الكتریكی محلول $HA$ از محلول $HX$ کمتر است.
اگر $A$ و $X$ هر دو هالوژن باشند، خاصیت نافلزی $A$ از $X$ کمتر است.
اگر مجموع غلظت یونها در محلول حاصل از حل کردن مقداری نیترو اسید $({{K}_{a}}=۴/۵\times {{۱۰}^{-۴}}mol.{{L}^{-۱}})$ در $۵۰۰$ میلیلیتر آب در دمای معین برابر $۰/۰۶$ مول بر لیتر باشد، جرم نیترو اسید اولیه به تقریب چند گرم است؟ (از تغییر حجم صرفنظر کنید؛ $H=۱,N=۱۴,O=۱۶~g.mo{{l}^{-۱}}$)


