 شرکت در آزمون آنلاین
شیمی 2
-
مسائل قانون هس
| آزمون شماره 3778
شرکت در آزمون آنلاین
شیمی 2
-
مسائل قانون هس
| آزمون شماره 3778
با توجه به واکنشهای داده شده، آنتالپی میعان بخار آب چند $kJ.mo{l^{ - 1}}$ است؟ \[\begin{array}{*{20}{l}}{C\,(S\,,\,{\rm{S\~A\^I Ho\neg }}) + 2{H_2}O(g) \to C{O_2}(g) + 2{H_2}(g)}&{\Delta {H_1} = + 163\,kJ}\end{array}\] (الف $\begin{array}{*{20}{l}}{{H_2}(g) + \frac{1}{2}{O_2}(g) \to {H_2}O(l)}&{\Delta {H_2} = - {{324}_/}1\,kJ}\end{array}$ (ب $\begin{array}{*{20}{l}}{2CO(g) + {O_2}(g) \to 2C{O_2}(g)}&{\Delta {H_3} = - 566\,kJ}\end{array}$ (ج $\begin{array}{*{20}{c}}{C(S\,,\,{\rm{S\~A\^I Ho\neg }}) + \frac{1}{2}{O_2}(g) \to CO(g)}&{\Delta {H_4} = - 121\,kJ}\end{array}$ (د
چنانچه آنتالپی تبخیر یک مول آب $42\,kJ$ باشد، آنتالپی واکنش $2{H_2}O(l) \to 2{H_2}(g) + {O_2}(g)$ چند کیلوژول است؟
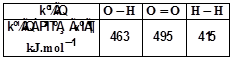
به کمک واکنشهای داده شده، محاسبه کنید که بهازای تشکیل 17 گرم هیدروژن پراکسید مایع، چند کیلوژول انرژی آزاد میشود؟ $(H = 1\,\,,\,\,O = 16:g.mo{l^{ - 1}})$ ${H_2}(g) + {O_2}(g) \to {H_2}{O_2}(l)$ $I)\,\,{N_2}{H_4}(l) + 2{H_2}{O_2}(l) \to {N_2}(g) + 4{H_2}O(l)\,\,\,\,\,\,\,\,\,\,\Delta {H_1} = - 818kJ$ $II)\,\,{N_2}{H_4}(l) + {O_2}(g) \to {N_2}(g) + 2{H_2}O(l)\,\,\,\,\,\,\,\,\,\,\Delta {H_2} = - 622kJ$ $III)\,\,{H_2}(g) + \frac{1}{2}{O_2}(g){H_2}O(l)\,\,\,\,\,\,\,\,\,\,\Delta {H_3} = - 285kJ$
با استفاده از واکنشهای زیر، \[\Delta H\] واکنش \[2\,A\,(g) \to B\,(g) + C\,(s)\] چند کیلوژول است؟ الف) \[E\,(g) + F\,(g) \to B\,(g)\,\,\,\,\,\,\,\,\Delta H = - 40\,kJ\] ب) \[G\,(g) + E\,(g) + F\,(g) \to C\,(g)\,\,\,\,\,\,\Delta H = - 110\,kJ\] ج) \[2\,F\,(g) \to A\,(g)\,\,\,\,\,\,\,\,\,\,\Delta H = - 58\,kJ\] د) \[2\,E\,(g) + G\,(g) \to 2\,F\,(g)\,\,\,\,\,\Delta H = - 115\,kJ\] هـ) \[C\,(s) \to C\,(g)\,\,\,\,\,\,\,\,\,\Delta H = 55\,kJ\]
با استفاده از واکنشهای داده شده، مقدار $\Delta H$ واکنش زیر را به دست آورید: \[{N_2}{H_4}\,(l) + {O_2}\,(g) \to {N_2}\,(g) + 2{H_2}O\,(l)\] $2\,N{H_3}(g) + 3{N_2}O\,(g) \to 4{N_2}(g) + 3{H_2}O\,(l)\,\,\,\,\,\,\,\,\Delta H = - 1010\,kJ\,$(1 ${N_2}O\,(g) + 3\,{H_2}(g) \to {N_2}{H_4}\,(l) + {H_2}O\,(l)\,\,\,\,\,\,\,\,\Delta H = - 318\,kJ\,$ (2 $2\,N{H_3}\,(g) + \frac{1}{2}\,{O_2}\,(g) \to {N_2}{H_4}\,(l) + {H_2}O\,(l)\,\,\,\,\,\,\,\Delta H = - 144\,kJ\,$ (3 ${H_2}\,(g) + \frac{1}{2}\,{O_2}\,(g) \to {H_2}O\,(l)\,\,\,\,\,\,\,\,\Delta H = - 286\,kJ\,$ (4


