 شرکت در آزمون آنلاین
شیمی 3
-
فصل 4: شیمی، راهی به سوی آینده ای روشن تر
| آزمون شماره 1112
شرکت در آزمون آنلاین
شیمی 3
-
فصل 4: شیمی، راهی به سوی آینده ای روشن تر
| آزمون شماره 1112
در اثر واکنش مقدار کافی پارازایلن \[({C_8}{H_{10}})\] با 100 میلیلیتر محلول \[{0_/}4\] مولار پتاسیم پرمنگنات \[(KMn{O_4})\] چند گرم ترفتالیک اسید \[({C_8}{H_6}{O_4})\] با درصد خلوص 83% تولید میشود؟ (بازده واکنش 80% بوده و سایر محصولات واکنش منگنز (IV) اکسید و پتاسیم هیدروکسید میباشند.) (\[O = 16,C = 12,H = 1:g.mo{l^{ - 1}}\])
چه تعداد از عبارتهای زیر در مقایسه واکنشهای سوختن فسفر سفید و هیدروژن در هوا و در دمای اتاق درست است؟
الف) هر دو واکنش در دمای اتاق، انجام شده و انرژی زیادی آزاد میکنند.
ب) انرژی فعال سازی واکنشی بیشتر خواهد بود که انرژی فعال سازی واکنش برگشت آن کمتر است.
پ) با فرض انجام دو واکنش و به ازای یک مول ماده اولیه، مقدار اکسیژن برابری مصرف خواهد شد.
ت) با فرض برگشت پذیر بود دو واکنش، انرژی فعال سازی واکنش برگشت سوختن هیدروژن کمتر است.
ثابت تعادل واکنش گازی: $۲{{H}_{۲}}(g)+{{S}_{۲}}(g)\rightleftharpoons ۲{{H}_{۲}}S(g)$ در دمای ${{۲۰۰۰}^{۰}}C$ برابر با $۱/۱\times {{۱۰}^{۲}}mo{{l}^{-۱}}.L$ است. یک مخلوط شامل ۰/۲ مول ${{H}_{۲}}S$، ۰/۰۰۲ مول ${{S}_{۲}}$ و ۲ مول ${{H}_{۲}}$ در یک ظرف دو لیتری در دمای ${{۲۰۰۰}^{۰}}C$ در حالت تعادل قرار ...................... و ............................
در مخلوطی از آلاینده ${{C}_{x}}{{H}_{y}}$ که از موتور خودرویی خارج میشود، دو نوع مولکول ${{C}_{۴}}{{H}_{y}}$ و ${{C}_{x}}{{H}_{۲۰}}$ به نسبت مولی یک به یک وجود دارد. اگر شمار مولهای اکسیژنی که برای حذف شانزده مول از مخلوط آلاینده موردنظر مصرف میشود، برابر $۱۶۰$ مول بوده و جرم کربن دی اکسید حاصل از واکنش منجر به حذف ${{C}_{x}}{{H}_{۲۰}}$، $۵۵$ برابر جرم آب حاصل از واکنش منجر به حذف ${{C}_{۴}}{{H}_{y}}$ باشد، مجموع $x$ و $y$ چند خواهد بود؟ $(H=۱,C=۱۲,O=۱۶:g.mo{{l}^{-۱}})$
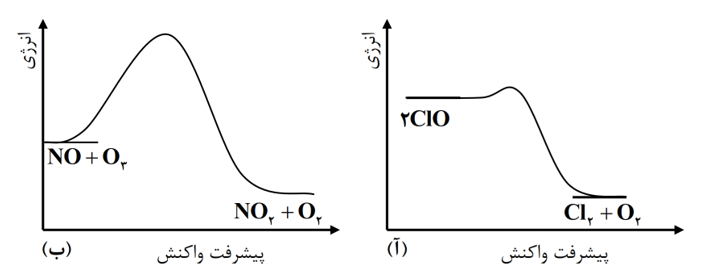 با توجه به نمودارهای زیر کدام عبارت درست است؟
با توجه به نمودارهای زیر کدام عبارت درست است؟


